|
Thông tin thuốc và phản ứng có hại của thuốc (ADR) (03/2024)
Nguồn:https://dhpp.hpfb-dgpsa.ca/reviewdocuments/resource/SSR1706035839788
I. Bộ Y tế Canada: Cảnh báo nguy cơ rối loạn chức năng mảnh ghép nguyên phát sau ghép tim liên quan đến sử dụng amiodaron
Bộ Y tế Canada phát hiện có mối liên quan giữa việc sử dụng amiodaron trước ghép tim và nguy cơ rối loạn chức năng mảnh ghép nguyên phát (PGD) sau ghép. Bộ Y tế Canada sẽ làm việc với các đơn vị sản xuất để cập nhật cảnh báo về nguy cơ trên vào thông tin các sản phẩm chứa amiodaron tại Canada.
Kết quả đánh giá an toàn:
- Bộ Y tế Canada đã tiến hành đánh giá các thông tin cung cấp từ các đơn vị sản xuất cũng như dữ liệu ghi nhận được từ cơ sở dữ liệu Cảnh giác dược Canada và trong y văn. Tại thời điểm đánh giá, Bộ Y tế Canada chưa ghi nhận bất cứ báo cáo nào về PGD có liên quan đến việc sử dụng amidaron trước ghép tim.
- Bộ Y tế Canada đã xem xét 7 ca PGD ở các bệnh nhân sử dụng amiodaron trước ghép tim đã được ghi nhận trên thế giới. Trong 7 ca, chưa thể xác định được vai trò của amiodaron do thiếu dữ liệu lâm sàng về các yếu tố nguy cơ khác, bao gồm thuốc sử dụng đồng thời và tình trạng bệnh lý của bệnh nhân.
- Bộ Y tế cũng đánh giá 6 bài nghiên cứu trong y văn. Mặc dù còn tồn tại một số hạn chế bao gồm các yếu tố gây nhiễu và sai lệch, bằng chứng từ các bài nghiên cứu là đủ để chứng minh việc sử dụng amiodaron trước ghép tim làm tăng nguy cơ PGD.
Kết luận và khuyến cáo của Bộ Y tế Canada:
- Bộ Y tế Canada xác định có mối liên quan giữa việc sử dụng amiodaron trước ghép tim và nguy cơ PGD sau ghép.
- Bộ Y tế Canada sẽ làm việc với các đơn vị sản xuất để cập nhật cảnh báo về nguy cơ PGD vào thông tin các sản phẩm chứa amiodaron tại Canada.
- Bộ Y tế Canada khuyến cáo bệnh nhân và các nhân viên y tế báo cáo các phản ứng có hại liên quan đến sử dụng amiodaron cũng như các chế phẩm y tế khác đến Hệ thống Cảnh giác dược Canada.
- Bộ Y tế Canada sẽ tiếp tục giám sát thông tin an toàn vê amiodaron lưu hành ở Canada để xác định và đánh giá nguy cơ tiềm ẩn. Bộ Y tế Canada sẽ thực hiện các biện pháp phù hợp và kịp thời nếu phát hiện các nguy cơ an toàn mới.
II. BÁO CÁO ADR TẠI TTYT HUYỆN GÒ QUAO THÁNG 3/2023
Trong tháng 3/2024 không ghi nhận trường hợp xảy ra phản ứng có hại của thuốc (ADR).
III. THU HỒI GIẤY ĐĂNG KÝ LƯU HÀNH THUỐC, THU HỒI THUỐC LƯU HÀNH TRÊN THỊ TRƯỜNG THÁNG 3/2024
1. Căn cứ Công văn số: 624/SYT-NVYD của Sở Y tế ngày 05 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 1104/QĐ-SYT ngày 29/02/2024 của Sở Y tế thành phố Hồ Chí Minh.
Thu hồi 02 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm do Sở Y tế thành phố Hồ Chí Minh đã cấp (đính kèm danh sách) cho Công ty TNHH TM DV Mỹ phẩm Hoàng Dũng là tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường (địa chỉ: 41 Đường 3, Khu nhà ở Vạn Phúc 1, Phường Hiệp Bình Phước, TP. Thủ Đức, TP.HCM), nhà sản xuất là Công ty Cổ phần Dược Mỹ phẩm Hành Tinh Xanh (địa chỉ sản xuất: số 30 Tam Bình, Khu phố 8, Phường Hiệp Bình Chánh, TP. Thủ Đức, TP.HCM).
Lý do: Công ty TNHH TM DV Mỹ phẩm Hoàng Dũng có văn bản đề nghị thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
|
STT
|
Nhãn hàng
|
Tên sản phẩm
|
Số công bố
|
Ngày cấp số tiếp nhận
|
|
1
|
Faceplus+
|
Sữa rửa mặt ngừa mụn giảm nhờn
|
2176/22/CBMP-HCM
|
24/6/2020
|
|
2
|
Faceplus+
|
Sữa rửa mặt dưỡng mịn da se khít lỗ chân lông
|
2255/22/CBMP-HCM
|
01/7/2022
|
2. Căn cứ Công văn số: 834/SYT-NVYD của Sở Y tế ngày 21 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 805/QĐ-SYT ngày 18/3/2024 của Sở Y tế Hà Nội.
Thu hồi 21 sổ tiếp nhận Phiếu công bố sản phẩm mỹ phẩm do Công ty cổ phần sản xuất và thương mại Chara sản xuất và ủy quyền cho các tổ chức, cá nhân khác chịu trách nhiệm đưa sản phẩm ra thị trường: (có danh sách kèm theo).
Lý do thu hồi: Công ty cổ phần sản xuất và thương mại Chara chấm dứt ủy quyền và có văn bản đề nghị thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
.png)
3. Căn cứ Công văn số: 865/SYT-NVYD của Sở Y tế ngày 25 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 224/QĐ-SYT ngày 20/3/2024 của Sở Y tế An Giang.
Thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm như sau:
|
STT
|
Nhãn hàng
|
Tên sản phẩm
|
Số phiếu tiếp nhận công bố mỹ phẩm
|
Ngày cấp
|
|
1
|
L2
|
L2 Red Peel Serum
|
172/23/CBMP-AG
|
26/7/2023
|
- Tên Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty TNHH thương mại mỹ phẩm Liên Nguyễn. (Địa chỉ công ty chịu trách nhiệm đưa sản phẩm ra thị trường: Số 1045B, đường Lâm Quang Ky, phường An Hoà, thành phố Rạch Giá, tỉnh Kiên Giang, Việt Nam).
- Tên Doanh nghiệp sản xuất: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab. (Địa chỉ: Số 136-138-140, đường Dương Diên Nghệ, tổ 16, khóm Mỹ Thọ, phường Mỹ Quý, thành phố Long Xuyên, tỉnh An Giang).
- Lý do thu hồi: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab tự nguyện đề nghị thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm nêu trên.
4. Căn cứ Công văn số: 866/SYT-NVYD của Sở Y tế ngày 25 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 225/QĐ-SYT ngày 20/3/2024 của Sở Y tế An Giang.
Thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm như sau:
|
STT
|
Nhãn hàng
|
Tên sản phẩm
|
Số phiếu tiếp nhận công bố mỹ phẩm
|
Ngày cấp
|
|
1
|
Nashi
|
Perfect Whitening Ampoule
|
183/23/CBMP-AG
|
14/8/2023
|
- Tên Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty TNHH dịch vụ thương mại Ngọc Châu Cosmetics. (Địa chỉ: Số 4/8, khu phố 2, thị trấn Ba Tri, huyện Ba Tri, tỉnh Bến Tre, Việt Nam).
- Tên Doanh nghiệp sản xuất: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab. (Địa chỉ: Số 136-138-140, đường Dương Diên Nghệ, tổ 16, khóm Mỹ Thọ, phường Mỹ Quý, thành phố Long Xuyên, tỉnh An Giang).
- Lý do thu hồi: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab tự nguyện đề nghị thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm nêu trên.
5. Căn cứ Công văn số: 867/SYT-NVYD của Sở Y tế ngày 25 tháng 03 năm 2024 về việc đình chỉ lưu hành, thu hồi và tiêu hủy mỹ phẩm không đạt tiêu chuẩn chất lượng tại Công văn số 844/QLD-MP ngày 20/3/2024 của Cục Quản lý Dược.
Đình chỉ lưu hành, thu hồi trên toàn quốc lộ sản phẩm Kem dưỡng trắng da Young One - Hộp 1 lọ 20g; Số lô: TYO.0123; NSX: 05.01.2023; HSD: 05.01.2026; Số công bố: 001052/22/CBMP-HCM; Tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường, sản xuất: Công ty TNHH hóa mỹ phẩm Chi Chi, địa chỉ: 240/13/18D Nguyễn Văn Luông, phường 11, quận 6, Tp. Hồ Chí Minh.
Lý do thu hồi: Mẫu kiểm nghiệm không đạt tiêu chuẩn chất lượng do chứa thành phần chất bảo quản Propyl paraben không có trong thành phần công thức sản phẩm đã được cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
6. Căn cứ Công văn số: 868/SYT-NVYD của Sở Y tế ngày 25 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 226/QĐ-SYT ngày 20/3/2024 của Sở Y tế An Giang.
Thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm như sau:
|
STT
|
Nhãn hàng
|
Tên sản phẩm
|
Số phiếu tiếp nhận công bố mỹ phẩm
|
Ngày cấp
|
|
1
|
ILAKIA
|
CC CREAM 3 in 1
|
178/23/CBMP-AG
|
07/8/2023
|
- Tên Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty TNHH phát triển thương mại Bonjour La Victoire. (Địa chỉ công ty chịu trách nhiệm đưa sản phẩm ra thị trường: Số 53, đường 61, phường 10, quận 6, thành phố Hồ Chí Minh, Việt Nam).
- Tên Doanh nghiệp sản xuất: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab. (Địa chỉ: Số 136-138-140, đường Dương Diên Nghệ, tổ 16, khóm Mỹ Thọ, phường Mỹ Quý, thành phố Long Xuyên, tỉnh An Giang).
- Lý do thu hồi: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab tự nguyện đề nghị thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm nêu trên.
7. Căn cứ Công văn số: 869/SYT-NVYD của Sở Y tế ngày 25 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 227/QĐ-SYT ngày 20/3/2024 của Sở Y tế An Giang.
Thu hồi 06 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm như sau:
|
STT
|
Nhãn hàng
|
Tên sản phẩm
|
Số phiếu tiếp nhận công bố mỹ phẩm
|
Ngày cấp
|
|
1
|
GC
|
Acne Clearing Serum
|
209/23/CBMP-AG
|
24/08/2023
|
|
2
|
GC
|
Melasma Super Cream
|
210/23/CBMP-AG
|
24/08/2023
|
|
3
|
GC
|
Melasma Super Serum
|
211/23/CBMP-AG
|
24/08/2023
|
|
4
|
GC
|
Acne Clearing Cream
|
222/23/CBMP-AG
|
21/09/2023
|
|
5
|
GC
|
Hyalu B5 Cream
|
223/23/CBMP-AG
|
21/09/2023
|
|
6
|
GC
|
Peel Retinol
|
224/23/CBMP-AG
|
21/09/2023
|
- Tên Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty cổ phần Charme Perfume. (Địa chỉ: Số 311, đường Hoàng Văn Thụ, phường 2, quận Tân Bình, thành phố Hồ Chí Minh, Việt Nam).
- Tên Doanh nghiệp sản xuất: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab. (Địa chỉ: Số 136-138-140, đường Dương Diên Nghệ, tổ 16, khóm Mỹ Thọ, phường Mỹ Quý, thành phố Long Xuyên, tỉnh An Giang).
- Lý do thu hồi: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab tự nguyện đề nghị thu hồi 06 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm nêu trên.
8. Căn cứ Công văn số: 886/SYT-NVYD của Sở Y tế ngày 26 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 236/QĐ-SYT ngày 21/3/2024 của Sở Y tế An Giang.
Thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm như sau:
|
STT
|
Nhãn hàng
|
Tên sản phẩm
|
Số phiếu tiếp nhận công bố mỹ phẩm
|
Ngày cấp
|
|
1
|
Nzim
|
Pink Cloud Youth Serum
|
221/23/CBMP-AG
|
18/09/2023
|
- Tên Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty TNHH MTV Nzim Beauty Room. (Địa chỉ: số 46, đường Nguyễn Thông, phường 09, quận 3, thành phố Hồ Chí Minh, Việt Nam).
- Tên Doanh nghiệp sản xuất: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm Worldlab. (Địa chỉ: Số 136-138-140, đường Dương Diên Nghệ, tổ 16, khóm Mỹ Thọ, phường Mỹ Quý, thành phố Long Xuyên, tỉnh An Giang).
- Lý do thu hồi: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm Worldlab tự nguyện đề nghị thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm nêu trên.
9. Căn cứ Công văn số: 887/SYT-NVYD của Sở Y tế ngày 26 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 238/QĐ-SYT ngày 21/3/2024 của Sở Y tế An Giang.
Thu hồi 05 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm như sau:
|
STT
|
Nhãn hàng
|
Tên sản phẩm
|
Số phiếu tiếp nhận công bố mỹ phẩm
|
Ngày cấp
|
|
1
|
Glowave
|
Deep Clear Facial Cleanser
|
257/23/CBMP-AG
|
13/12/2023
|
|
2
|
Glowave
|
Gentle Clean For Men
|
258/23/CBMP-AG
|
13/12/2023
|
|
3
|
Glowave
|
Bright Body Tone Up Cream
|
266/23/CBMP-AG
|
14/12/2023
|
|
4
|
Glowave
|
Silky Whitening Body Cream
|
268/23/CBMP-AG
|
14/12/2023
|
|
5
|
Glowave
|
Himalaya Body Scrub
|
277/23/CBMP-AG
|
22/12/2023
|
- Tên Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty TNHH mỹ phẩm Minh Khang. (Địa chỉ: số 231 đường số 1, phường 11, quận Gò Vấp, thành phố Hồ Chí Minh, Việt Nam).
- Tên Doanh nghiệp sản xuất: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab. (Địa chỉ: Số 136-138-140, đường Dương Diên Nghệ, tổ 16, khóm Mỹ Thọ, phường Mỹ Quý, thành phố Long Xuyên, tỉnh An Giang).
- Lý do thu hồi: Công ty TNHH phát triển thương mại sản xuất dược mỹ phẩm worldlab tự nguyện đề nghị thu hồi 05 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm nêu trên.
9. Căn cứ Công văn số: 888/SYT-NVYD của Sở Y tế ngày 26 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 1758/QĐ-SYT ngày 21/3/2024 của Sở Y tế thành phố Hồ Chí Minh.
Thu hồi 01 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm do Sở Y tế thành phố Hồ Chí Minh đã cấp (đính kèm danh sách) cho Công ty TNHH Salacos là nhà sản xuất đồng thời cũng là tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường (địa chỉ: D3/492K Đường Vườn Thơm, Xã Bình Lợi, Huyện Bình Chánh, thành phố Hồ Chí Minh).
Lý do: Công ty TNHH Salacos có văn bản đề nghị thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
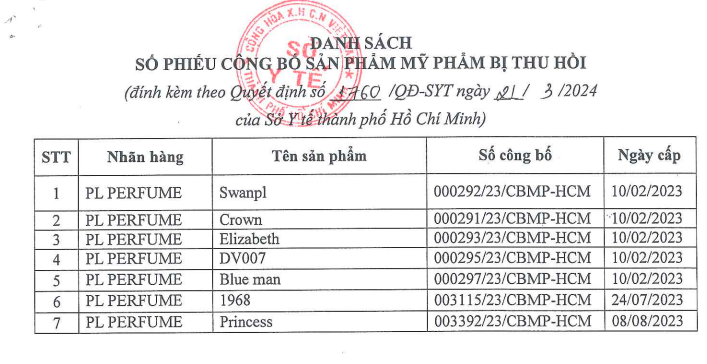
10. Căn cứ Công văn số: 889/SYT-NVYD của Sở Y tế ngày 26 tháng 03 năm 2024 về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại Quyết định số 1760/QĐ-SYT ngày 21/3/2024 của Sở Y tế thành phố Hồ Chí Minh.
Thu hồi 07 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm do Sở Y tế thành phố Hồ Chí Minh đã cấp (đính kèm danh sách) cho Công ty TNHH Đầu tư và Phát triển Xuất nhập khẩu Thịnh Phát là tổ chức chịu trách nhiệm đưa sản phẩm mỹ phẩm ra thị trường (địa chỉ: Số 9 Đường số 4, Khu dân cư Conic, Xã Phong phú, Huyện Bình Chánh, TP.HCM), Chi nhánh Công ty Cổ phần Sản xuất Dược Mỹ phẩm Hataphaco là nhà sản xuất (địa chỉ: 5B Đường An Hội, Phường 13, Quận Gò Vấp, TP.HCM);
Lý do: Công ty TNHH Đầu tư và Phát triển Xuất nhập khẩu Thịnh Phát có văn bản đề nghị thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
|